Access to Treatment 古くて新しい病気「結核」に立ち向かう
結核治療薬デラマニドで世界の公衆衛生を改善
結核は、紀元前に埋葬されたミイラでも見られるように*1、長い間人々を苦しめ続けています。
結核は現在、新型コロナウイルス感染症に次いで、世界での年間死者数の多い感染症です*2,3。近年の薬剤耐性株の蔓延は、さらにその死亡率を高めています。
しかし、結核は治療も予防も可能な疾患です。大塚製薬は、結核治療薬デラマニドを世界に展開し、結核の撲滅を目指しています。
*1 Thomas M. Daniel (2006)
*2 World Health Organization. Global tuberculosis report 2020
*3 World Health Organization. Coronavirus disease (COVID-19) dashboard
結核とは?
結核は世界で最も深刻な感染症の一つで、空気感染によって結核菌が体に入って主に肺で増殖し、咳や痰等の症状を引き起こします。深刻化すると、呼吸が困難になったり、他の臓器などにも影響したりして、最終的には死に至ることもあります。感染力は強い一方、発症するのは生涯を通して5~10%程度といわれ、体力の低下や加齢などにより、感染後何年もたってから発症するケースもあります。
多剤耐性と超多剤耐性結核
1990年代以降、結核治療薬に対し広く耐性を有した結核菌が蔓延しています。不規則な服用や副作用等による服薬中断により、服用中の薬に対する耐性を持った結核菌が生まれます。中でも、最も強力な治療薬であるリファンピシンとイソニアジドに対して耐性を持つようになったのが、多剤耐性結核菌です。また、さらに多くの結核治療薬に対する耐性を有する超多剤耐性結核菌も出現し、結核撲滅に向けた取り組みの上で世界的に大きな課題となっています。
SDGs target 3.3
2015年、国連は持続可能な開発目標(SDGs)を採択しました。SDG3は公衆衛生への取り組み、SDG3.3では、2030年までに、エイズ、結核、マラリアおよび顧みられない熱帯病といった伝染病を根絶するとともに肝炎、水系感染症およびその他の感染症に対処することが掲げられています。
しかし、ストップ結核パートナーシップが発表した推計*4では、新型コロナウイルス感染拡大により結核高蔓延国における医療体制が影響を受けているため、SDGsにより掲げられた2030年の目標は少なくとも5年以上遅延する可能性が示唆されています。
*4 “TB and COVID-19” Stop TB Partnership website, available at: http://www.stoptb.org/covid19.asp
結核菌の保有者数 約17億人
結核による年間死亡者数 約150万人
現在でも世界で蔓延する結核
結核は非常に感染力の強い病気で、世界中で17億人程度は結核菌の保菌者であるといわれています。2020年には約990万人が発症し、約150万人の方が亡くなっています*5。
結核は多くの低・中所得国で蔓延しており、長期間にわたる治療が必要であるため、経済的にも大きな課題となっています。
*5 World Health Organization. Global Tuberculosis Report 2021
従来の治療の限界
結核を引き起こす結核菌は非常に「しぶとい菌」です。
現在の治療では、耐性菌の出現を抑えるため、3~4種類の治療薬が投与されています。多くの場合、どの薬剤にも耐性化していない結核は、「一次抗結核薬」と呼ばれる薬剤群の投与と適切な管理により、治療を成功させることができます。しかしながら、より危険な多剤耐性や超多剤耐性結核に対しては「二次抗結核薬」と呼ばれる薬剤群が投与され、これらの組み合わせにおいてデラマニドは使用されます。
社会課題の解決に寄与するデラマニド
40年ぶりの新薬が生まれるまで
デラマニド誕生ストーリー
―誰もがやらないなら、大塚がやらなくては―
デラマニドは、2014年に多剤耐性肺結核の適応で承認されました。本剤は、これまでの治療薬とは全く異なる作用機序を持ち、既存の治療薬に耐性のある結核菌に対しても効果があります。そのため、深刻化する多剤耐性結核に対する治療薬としての役割が期待されており、2015年にはWHOの必須医薬品モデル・リスト(どの国でも最小限必要とされる医薬品のリスト)に掲載されています。
デラマニドは、世界でほぼ40年ぶりに承認された結核治療薬の一つです。今でこそ多剤耐性結核が注目されていますが、1964年に結核の標準治療薬リファンピシンの発見以降、つい最近まで結核はすでに克服された病気と思われていました。1970年代には世界中の研究者や研究機関の多くが開発を中止するなか、大塚は「結核は重大なグローバルヘルスの問題。誰もがやらないなら、我々が研究を続けなければならない」との想いで研究を継続。30年を超える研究の成果がデラマニド誕生につながりました。
大塚製薬は、現在でも新たな結核治療薬の研究開発に積極的に取り組んでおり、10年以上にわたり、結核分野での研究開発に最も投資を行っている企業の一つに位置付けられています。
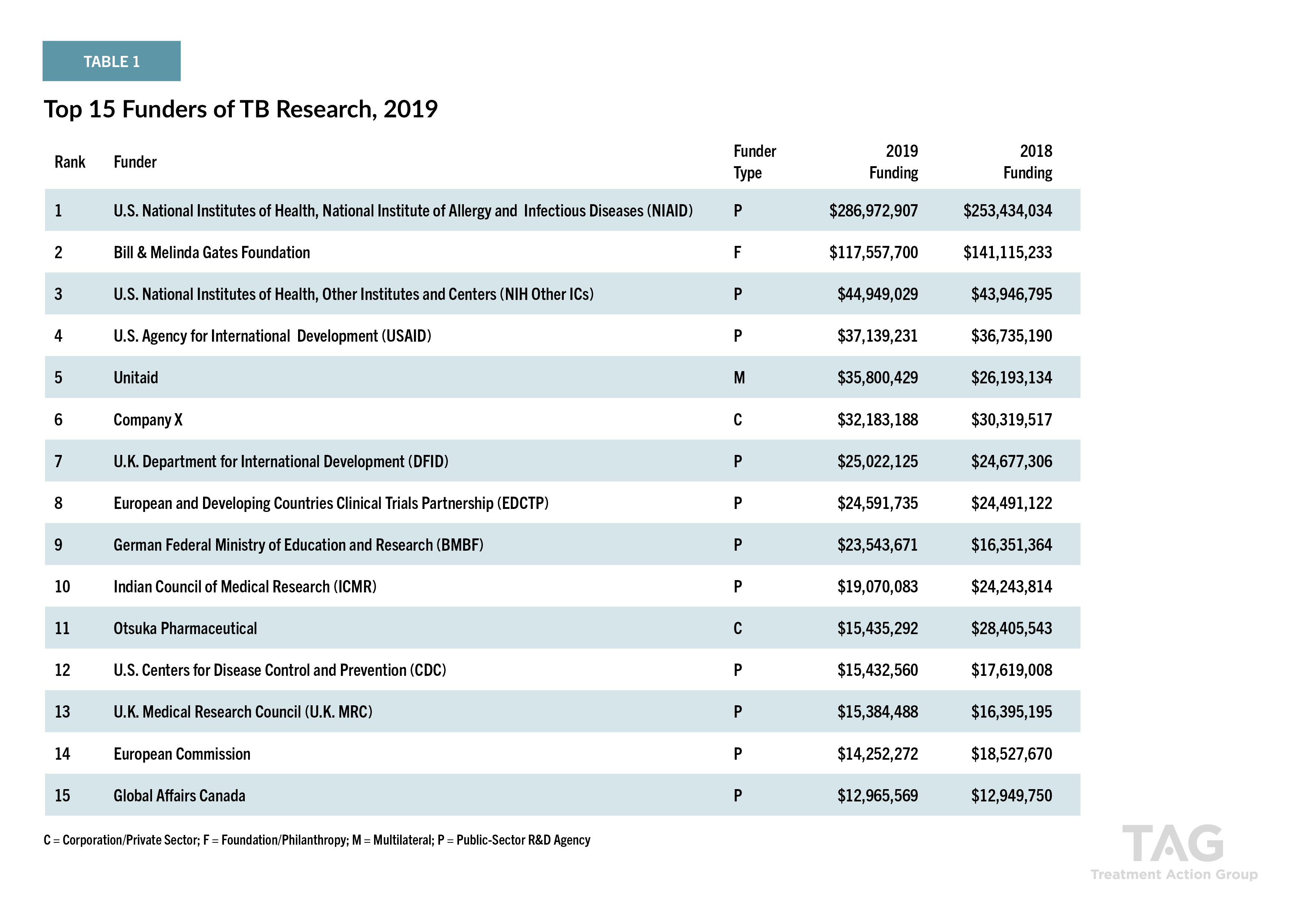
Tuberculosis Research Funding Trends 2005 – 2019, Stop TB Partnership and Treatment Action Group
大塚の結核研究の軌跡
| 1971 | 大塚製薬が創薬研究を開始、感染症をテーマの一つとして取り組む |
|---|---|
| 2002 | 結核治療薬候補となる化合物を発見 |
| 2004 | 開発コードOPC-67683(後のデラマニド)が結核を対象とする第一相臨床試験が開始 |
| 2008 | 多剤耐性結核の患者さんを対象としたデラマニドの第二相臨床試験が開始 |
| 2011 | 多剤耐性結核の患者さんを対象としたデラマニドの第三相臨床試験が開始 |
| 2013 | 小児の多剤耐性結核の患者さんを対象としたデラマニドの臨床試験が開始 |
| 2014 | デラマニドが多剤耐性肺結核治療薬「デルティバ」として、欧州および日本で承認・販売開始 |
| 2016 | 新規結核治療薬候補OPC-167832の第一相臨床試験が開始 |
| 2018 | OPC-167832の第一/二相臨床試験が開始 |
| 2020 | 業種の枠を超えた世界初のコラボレーションPAN-TB Collaborationに参画 |
小児結核への取り組み
毎年、25,000人から30,000人の子供たちが多剤耐性結核を発症しています*6。このうち、診断され治療を受けることができるのはわずか3~4%であり、約21%の子供たちが亡くなっています*7。
多剤耐性結核の治療は困難であり、その中でも小児の治療はより困難です。そこで、小児患者さん向けのデラマニドの新剤型を開発し、体重10kg以上の小児患者さんでの使用が2021年9月に欧州委員会から承認されました。
*6 Access to Medicine Foundation report "Tuberculosis in Children: Underdiagnosed and Undertreated" (2020)
*7 Helen E Jenkins and Courtney M Yuen (2018)
社会との協働を図る
ストップ結核パートナーシップの世界抗結核薬基金(Stop TB Partnership/Global Drug Facility)と協働して、デラマニドのアクセスを低所得国に拡大

40年ぶりの新薬の一つとして承認されたデラマニドですが、患者さんの元に届かなくては意味がありません。しかし、大塚製薬が拠点を持たないアフリカやアジアなどの途上国に多くの患者さんがいます。品質が保証された結核治療薬や診断薬へのアクセスを拡大し、途上国での持続可能な調達を可能とした組織であるストップ結核パートナーシップの「世界抗結核薬基金(GDF:Global Drug Facility)*8」とパートナーシップを結びました。GDFを通じたデラマニドの供給国は80以上になります。現在デラマニドを服用している患者さんの多くはGDFが調達した薬剤を使用しており、アクセス拡大の大きな支援となっています。
*8 2001年に設立以降、ストップ結核パートナーシップは、結核に対する感染リスクの高いすべての人々に対し、質の高い診断、治療、ケアの提供をサポートすることを使命としています。GDFは、公共セクターに対する品質の確かな結核治療薬、診断薬、検査用品の世界最大の供給者であり、結核対策プログラムへの技術援助や、革新的なツールの普及支援を行っています。
StopTB/GDFを通じた「デルティバ」の供給ルート
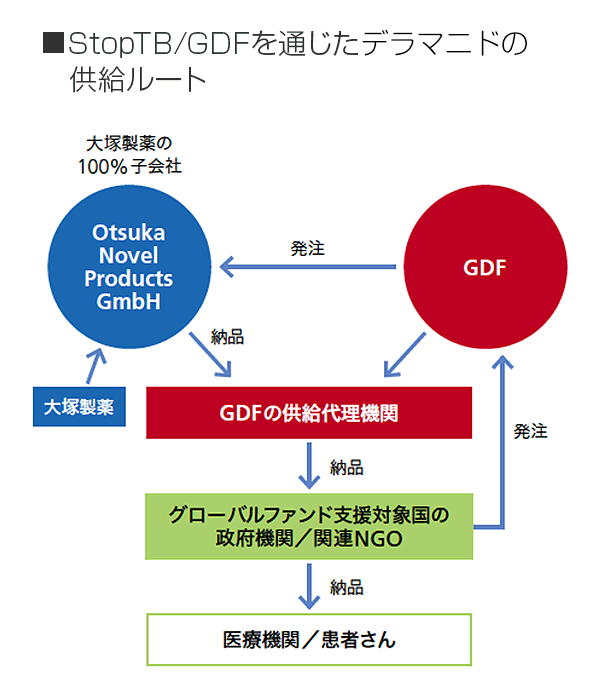
デラマニドに関する日本政府との協力

アクセス拡大に向けて海外での早期承認への要望や国際会議での発言など日本政府とも協力し、また様々な支援を受けています。

日露首脳が合意した8項目の経済協力プランの一つが医療の向上と健康寿命の増進。2017年9月7日、ウラジオストクで開催された東方経済フォーラムにて、当時安倍晋三首相がデラマニドのロシアでの早期承認に向けた両国の協力について『日露が手を結ぶ、結核との闘いです』とスピーチされました。
2018年9月26日、ニューヨークで開催された国連総会結核ハイレベル会合にて加藤勝信厚生労働大臣が、日本発の多剤耐性結核治療薬の開発と世界の結核撲滅に向けた貢献についてスピーチされました。また同時に、結核撲滅に向けた政治宣言が採択されました。
世界中の患者さんを救う供給ネットワークの構築
世界中の患者さんへアクセス拡大

結核のようなグローバルヘルスの課題となる疾患に対しては、WHOや国連・各国政府が積極的な支援を行っており、多くのパートナーシップが存在します。
大塚製薬では、GDFとのパートナーシップ以外にも、世界の感染症制圧に向け設立された日本の官民パートナーシップ「公益社団法人グローバルヘルス技術振興基金(GHIT)」への参加や、「国境なき医師団(MSF)」等が展開するプログラムへの協力、新しい結核治療方法の開発に向けた「ビル&メリンダ・ゲイツ財団」の支援獲得、自社が拠点を持たない地域や公衆衛生に強みを持つグローバル企業(インド・ヴィアトリス社、ロシア・アールファーム社)とのアライアンス等、多くのステークホルダーを巻き込んだ活動を通じて、世界の人々の健康に貢献するための取り組みを行っています。
大塚製薬が参画するイニシアチブ等
Rome 5
歴史的にHIV感染の小児にフォーカスしてきたバチカン市国の取り組み。現在は結核にも注力しています。
Ending Workplace TB
働く環境における結核の感染をなくすため、世界経済フォーラム、世界基金、民間企業が協業しています。大塚製薬は、社内外のコミュニケーション活動を通じて、結核高蔓延国の一般市民や自社の従業員に対して結核への理解を深める活動を行っています。
デラマニドの世界におけるアクセスを推進するため、インドや南アフリカについてはヴィアトリス社と、ロシアやCIS諸国についてはアールファーム社と提携するなど、公衆衛生やグローバル展開に強みを持つ様々な企業と協業しています。また、適正な価格でのアクセスを確保するため、インドでの生産を目指し、ヴィアトリス社への製造技術の移管作業を進めています。
2017年3月には、南アフリカ政府と協力の上、多剤耐性肺結核の患者さんにデラマニドを薬事承認前にいち早く届けるための国家プログラム「デラマニド臨床アクセスプログラム」を開始しました。現在では南アフリカにおいても正式に承認され、より多くの患者さんに使用されるようになりました。
大塚製薬では、デラマニドを必要とする世界の患者さんが各国の社会・経済状況や所得水準に関係なく治療を受けられるよう、適正な価格による持続可能な薬剤提供体制の構築に取り組んでいます。このような多角的なアプローチによって、2021年には110を超える国々でデラマニドの使用が推し進められています。
継続した結核治療薬探索への取り組み
次世代の結核治療薬候補「OPC-167832」
大塚製薬はデラマニドに続く結核治療薬の研究を進めています。その「OPC-167832」は大塚製薬が独自に創製した新規化合物で、2021年現在、南アフリカで薬剤の効果を確認する第二相臨床試験開始が進行しています。この化合物は結核菌の細胞壁を合成するために必須となる、デラマニドとは異なる酵素の活性を阻害する仕組みで結核菌を死滅させます。既存の結核治療薬と全く異なる作用機序を持つため、次世代の治療薬として期待されています。開発にあたっては、世界の結核撲滅を最重要課題の一つに掲げている「ビル&メリンダ・ゲイツ財団」からの支援も受け、新たな治療方法の確立に向けて開発を進めています。
大塚が参画するイニシアチブ等
The Project to Accelerate New Treatments for Tuberculosis (PAN-TB)
すべての結核を治療できる治療レジメン(PAN-TBレジメン)の開発を加速することを目的とした、ビル&メリンダ・ゲイツ財団を中心とした慈善団体、非営利団体、民間企業が協力する初のプロジェクト
EU-PEARL
臨床試験をより効率的に、また患者さん中心的に変革していく取り組み
Unite4TB
新規結核治療薬の開発を促進するための欧州革新的医薬品イニシアティブ(IMI)が支援する官民共同のプロジェクト
薬剤耐性(AMR)問題への取り組み
2050年までに、薬剤耐性結核による死亡者数は年間250万人に達する可能性が示唆されています*9。大塚製薬は、デラマニドに対する耐性菌の出現を防ぐべく責任のあるアクセスプログラム(Responsible Access Program : RAP)を策定し、デラマニドの適正使用を進めています。
これらの適正使用に対する体制や、グローバルアクセスへの取り組み、そして薬剤耐性結核に対する継続的な研究開発の推進は、イギリスとオランダの政府などが資金を提供するAccess to Medicine Foundationが発行し、世界の製薬会社30社を対象としたAMRベンチマークにおいても評価されています*10。
*9 The Review on Antimicrobial Resistance. Tackling drug-resistant infections globally: Final report and recommendations. London: Wellcome Trust and HM Government, 2016. Available from:
https://amr-review.org/sites/default/files/160525_Final%20paper_with%20cover.pdf
*10 https://accesstomedicinefoundation.org/amr-benchmark

